コンテンツ
ヒアルロン酸ナトリウムの溶液であるSupartzは、粘性補充で使用されるヒアルロン酸塩の1つです。 Supartzは膝関節に直接注入され、滑液(関節液)のクッション性と潤滑性を回復します。Supartzで使用されるヒアルロン酸ナトリウムは、鶏の櫛から抽出されます。ヒアルロン酸ナトリウムは、グルクロン酸とN-アセチルグルコサミンの繰り返し二糖単位を含む多糖です。
関節潤滑剤注射は関節炎の効果的な治療法ですか?SupartzおよびSupartz Fxの承認
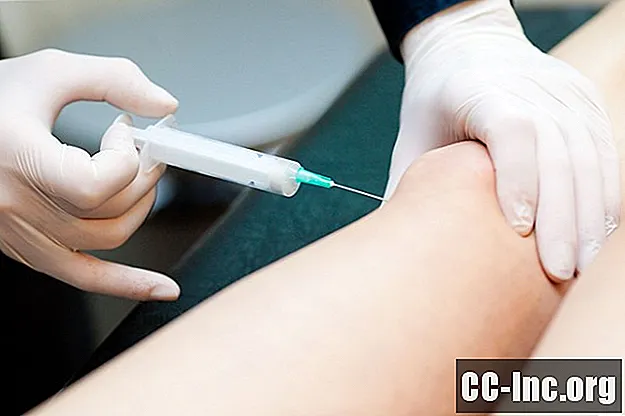
Supartzは、2001年1月24日に、運動、理学療法、鎮痛剤、移動補助器具、ホットパックまたはコールドパックなどの保存的治療で十分な緩和が得られなかった患者の変形性膝関節症の治療について、米国FDAによって承認されました。他の関節の使用が調査されています。 Supartzは1987年から日本で使用されています。5週間のサイクルで週に1回注射されます。一部の患者は3週間後に良好な反応が見られる場合があります。
2015年10月12日、SupartzのメーカーであるBioventusは、Supartz Fx(1.0%生理食塩水に溶解した10 mgのヒアルロン酸ナトリウム)の発売を発表しました。注射の繰り返しサイクルのために安全ラベルが拡張されましたが、繰り返しサイクルの有効性は確立されていません。
Supartzの警告と注意
Supartzは、ヒアルロン酸ナトリウム製品に対する過敏症が知られている患者には投与しないでください。鳥類のタンパク質、卵、または羽に対して既知のアレルギーを持つ患者を治療する場合は注意が必要です。注射が行われる領域に感染症または皮膚疾患がある患者は、スパルツで治療すべきではありません。
Supartzの安全性と有効性は、妊婦でも授乳婦でも確立されていません。その使用は子供で研究されていません。
Supartz注射の一般的な副作用
Supartzに関連する一般的な副作用または有害事象は次のとおりです。
- 炎症のない関節痛
- 背中の痛み
- 非特異的な痛み
- 注射部位反応
- 頭痛
一時的な腫れや痛みは、Supartzを注射した関節に発生する可能性があります。
患者は、注射後48時間は激しいまたは体重を支える活動を避けるようにアドバイスされています。
結論
5つの適切に設計された臨床試験の分析では、有害事象に関してSupartz群と対照群の間に有意差は見られませんでした。Supartzと他の粘液サプリメントの安全性は臨床研究によって支持されてきましたが、有効性については議論されています。
有効性に関して、Cochrane Reviewはビスコサプリメントがプラセボより効果的であると結論付けましたが、注射が有意な痛みの軽減を提供することを証明するのに不十分な他の研究がありました。
- 共有
- フリップ
- Eメール
- テキスト